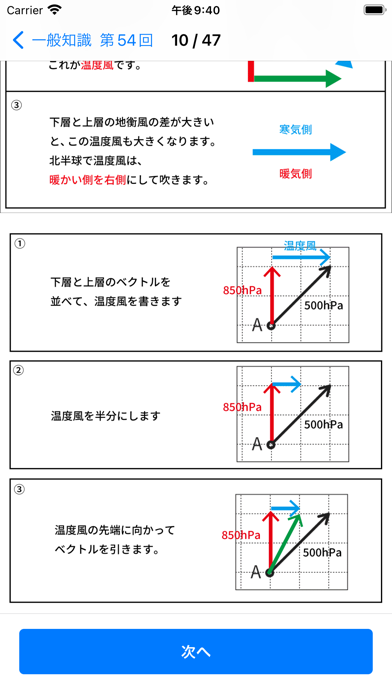
シャルルの法則とボイルの法則
状態方程式 P = ρ × R × T の中で、ある変数を一定に固定すると、残りの変数の間にシンプルな関係が見えてきます。
シャルルの法則(気圧一定のとき)
気圧 P を一定とすると、気体定数 R も一定なので、変化するのは密度 ρ と絶対温度 T の2つだけになります。
このとき、密度と絶対温度は反比例の関係にあります。つまり、
- 密度が大きくなると → 絶対温度は低くなる
- 密度が小さくなると → 絶対温度は高くなる
これをシャルルの法則といいます。
日常的な意味
気圧が同じ条件で比べたとき、暖かい空気は密度が小さく軽い、冷たい空気は密度が大きく重いということです。
熱気球が空を飛べるのはまさにこの原理です。バーナーで空気を暖めると密度が小さくなり(軽くなり)、周囲の冷たい空気より浮力が生じて上昇するのです。
ボイルの法則(絶対温度一定のとき)
絶対温度 T を一定とすると、変化するのは気圧 P と密度 ρ の2つだけになります。
このとき、気圧と密度は比例の関係にあります。つまり、
- 密度が大きくなると → 気圧も大きくなる
- 密度が小さくなると → 気圧も小さくなる
これをボイルの法則といいます。
日常的な意味
温度が同じ条件で比べたとき、密度が小さい(軽い)空気は気圧が小さい、密度が大きい(重い)空気は気圧が大きいということです。
ボイル=シャルルの法則
状態方程式全体を指して、ボイル=シャルルの法則とよぶこともあります。
比例と反比例のまとめ
| 関係 | 意味 |
|---|---|
| 比例 | 一方が大きくなると、もう一方も大きくなる |
| 反比例 | 一方が大きくなると、もう一方は小さくなる |
| 2乗に比例 | 一方が2倍になると、もう一方は4倍(2²)になる |
| 2乗に反比例 | 一方が2倍になると、もう一方は1/4(1/2²)になる |
分圧と全圧
空気はいくつかの気体の混合物です。気圧を個々の気体ごとの圧力に分けて考えることができます。
- 分圧:気圧を個別の気体の圧力に分けたもの
- 全圧:すべての分圧を足し合わせたもの(= 気圧)
たとえば地上の気圧が約1000hPaの場合、窒素の分圧は約800hPa(約80%)、酸素の分圧は約200hPa(約20%)となります。